然而,一系列的调查、指控和令人失望的临床试验结果揭露了其背后的学术不端行为,最终导致该药物的陨落。其背后的真相也是让人吃惊。
科学家王厚炎
故事的中心人物是神经科学家王厚炎(Hoau-Yan Wang),他曾是纽约市立大学 (CUNY) 的终身教授,也是 Cassava Sciences 公司的长期顾问和 Simufilam 药物的主要开发者之一。
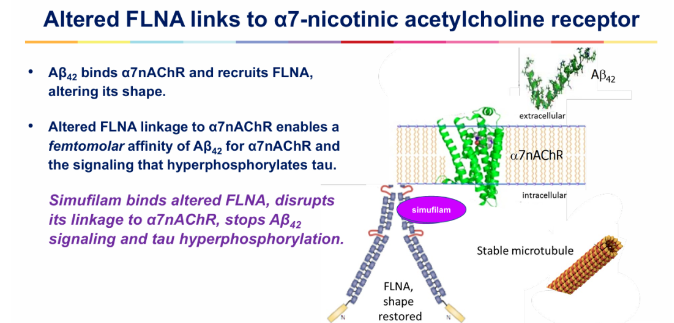
王厚炎与 Cassava 公司高级副总裁 Lindsay Burns 合作,对 Simufilam 进行了大量的研究,并在多个期刊上发表了支持该药物疗效的论文。其中包括 2012 年发表在《神经科学杂志》上的一篇关键论文,该论文声称 Simufilam 可以减少 β-淀粉样蛋白的毒性作用,而 β-淀粉样蛋白在大脑中的异常积聚被广泛认为是阿尔茨海默病的病因。

然而,从 2021 年开始,王厚炎的研究就遭到了质疑。
两位神经科学家 Geoffrey Pitt 和 David Bredt 向美国食品药品监督管理局 (FDA) 提交了一份请愿书,要求暂停 Simufilam 的临床试验,理由是王厚炎的多篇论文中存在图像篡改的迹象,这些迹象削弱了 Simufilam 能够减缓甚至逆转阿尔茨海默病症状的说法。
随后,美国国立卫生研究院 (NIH) 将这些指控转交给了研究诚信办公室 (ORI),ORI 随后联系了王厚炎所在的纽约市立大学 (CUNY) 展开调查。
CUNY 的调查委员会审查了王厚炎在 2003 年至 2021 年期间发表的论文、会议海报和 NIH 拨款申请,并在 2023 年 5 月完成了一份长达 50 页的报告,指控王厚炎在 20 篇研究论文中存在学术不端行为,包括图像篡改。
为了核实这些数据的真实性,调查委员会试图获取原始数据图像,但王厚炎未能提供任何原始数据。
调查委员会还发现,王厚炎将蛋白质印迹图的制备工作“严格地孤立”起来,几乎所有的图像都是由他自己制作的,这对于一个实验室的首席研究员来说是非常奇怪的。
面对这些指控,王厚炎提出了各种辩解,包括声称包含关键数据的硬盘被 CCNY 的官员销毁,以及指责调查委员会对他有偏见,不懂什么是WB。
不懂WB?调查委员会相关人员直接说,自己经常进行涉及蛋白质生物化学的实验,而且经常做蛋白质印迹实验。CUNY 的调查报告最终得出结论,王厚炎在数据管理和记录保存方面存在“长期且严重的学术不端行为。
FDA 的介入:实验室调查揭露更多问题
2020 年 5 月,该公司公布了一项 2 期临床试验的结果,结果令人失望。该药物未能降低该疾病的关键标志物的水平。该公司股价一夜之间下跌了四分之三。
然而,几个月后,Cassava 公司在一份新闻稿中否定了这些令人失望的结果:suggesting a contractor had analyzed patient samples improperly。
该公司提供了一项为期 28 天、涉及 64 名阿尔茨海默病患者的研究的更好消息,其中包括一组服用安慰剂的患者。这一次,Simufilam 显著降低了 tau 蛋白、β-淀粉样蛋白和其他生物标志物的水平。
Cassava 公司的股价立即上涨了一倍多,一些生物技术分析师对该药物的前景变得更加乐观。
2022 年 9 月,FDA 官员前往 CUNY 的一个研究中心,计划审查王厚炎实验室的记录和操作规范。起初CUNY 拒绝了 FDA 调查人员的进入,保安甚至将他们赶走。两天后,当 CUNY 最终允许 FDA 进入实验室时,工作人员发现王厚炎在之前的工作中存在一系列问题。
FDA 的调查主要集中在王厚炎对 Simufilam 临床试验样本的处理方式上,调查人员发现王厚炎在处理异常数据时存在严重问题。他声称自己根据判断剔除异常值,但 FDA 调查人员发现他没有预先设定明确的标准。此外,他们独立审查了王厚炎的数据,发现了更多错误。
深入调查后发现他从未对设备进行例行校准,也没有完成验证实验以确保测试的准确性、灵敏度和精确度。还使用了不恰当的统计测试,导致样本浓度测定不准确。
在一系列调查之后,王厚炎于 2023 年 6 月被美国司法部 (DOJ) 起诉,罪名是“诈骗美国国立卫生研究院 (NIH) 约 1600 万美元的拨款”。
DOJ 指控王厚炎在 2015 年 5 月至 2023 年 4 月期间“参与了一项在代表自己和生物制药公司提交给 NIH 的拨款申请中伪造和篡改科学数据的计划”。如果罪名成立,王厚炎将面临最高 10 年的监禁。
Cassava Sciences :深陷泥潭
Cassava Sciences 是 Simufilam 的开发公司,该公司及其高管也卷入了这场丑闻。
美国证券交易委员会 (SEC) 在 2023 年 9 月指控 Cassava 公司误导投资者,称该公司及其两名前高管(前首席执行官 Remi Barbier 和神经科学高级副总裁 Lindsay Burns)在 Simufilam 的早期临床结果方面误导了投资者。
SEC 的投诉指出, Barbier 知道王厚炎的实验室不具备进行生物标志物测试的资格,而这些测试表明 Simufilam 对阿尔茨海默病有效。SEC 还指控王厚炎在测试患者液体样本时“未被蒙蔽”,这意味着他知道哪些患者服用该药物,哪些患者服用安慰剂,这可能会导致他的数据产生偏差。
最终,Cassava 公司同意支付 4000 万美元与 SEC 达成和解。Barbier 和 Burns 也分别同意支付 17.5 万美元和 8.5 万美元的罚款,并将分别被禁止担任公司高管和董事 3 年和 5 年。
此外,王厚炎同意支付 5 万美元以了结相关行政程序中的指控。
Cassava 公司在多大程度上参与了王厚炎的学术不端行为? 可能知晓或默许了王厚炎的数据问题,但仍然将这些数据作为 Simufilam 疗效的证据。 SEC 的指控也表明,Cassava 公司及其高管在误导投资者方面负有责任。
该公司只有一种药物正在开发中,这使其未来充满了不确定。三期临床失败消息传出后,其股价暴跌超过 80%,市值下跌约 10 亿美元。

发表评论